
O conceito de equilûÙbrio quûÙmico estûÀ relacionado û capacidade de um sistema quûÙmico de manter as concentraûÏûçes dos reagentes e...

O conceito de equilûÙbrio quûÙmico estûÀ relacionado û capacidade de um sistema quûÙmico de manter as concentraûÏûçes dos reagentes e produtos constantes ao longo do tempo, quando estûÀ em um estado de equilûÙbrio dinûÂmico. Entender as constantes de equilûÙbrio (Kc e Kp) e os fatores que podem influenciar o equilûÙbrio, como temperatura, pressûÈo e concentraûÏûÈo ûˋ fundamental para um bom desempenho no Enem e vestibulares.
O conceito de equilûÙbrio quûÙmico ûˋ fundamental para estudantes que se preparam para o Enem e vestibulares. Este tû°pico estûÀ relacionado û capacidade de um sistema quûÙmico de manter as concentraûÏûçes dos reagentes e produtos constantes ao longo do tempo, quando estûÀ em um estado de equilûÙbrio dinûÂmico. No contexto dos estudos preparatû°rios, ûˋ importante que os alunos compreendam os principais tipos de equilûÙbrio e as fû°rmulas relacionadas, o que lhes permitirûÀ resolver questûçes de quûÙmica com confianûÏa. Ao estudar equilûÙbrio quûÙmico, os estudantes devem focar em entender a lei da aûÏûÈo das massas, as constantes de equilûÙbrio (Kc e Kp) e os fatores que podem influenciar o equilûÙbrio, como temperatura, pressûÈo e concentraûÏûÈo. Esses conceitos sûÈo essenciais para desenvolver uma base sû°lida em quûÙmica e para o desempenho nos exames de admissûÈo, permitindo que os estudantes interpretem e analisem problemas complexos com eficûÀcia.
O fascinante mundo do equilûÙbrio quûÙmico responde a perguntas como por que um refrigerante libera gûÀs quando aberto ou como o nosso sangue consegue transportar oxigûˆnio sem “despejûÀ-lo” todo de uma vez.
O equilûÙbrio quûÙmico ûˋ, portanto, um dos pilares daô quûÙmicaô e, tambûˋm um dos tû°picos mais recorrentes e desafiadores noô Enem.
Dados mostram que o assunto aparece em aproximadamenteô 80% das provasô do exame nacional, o que significa que dominûÀ-lo ûˋ um passo estratûˋgico e fundamental para a sua aprovaûÏûÈo.
Tendo isso em consideraûÏûÈo, ao longo deste artigo, vamos desvendar esseô conceito e exploraremos desde as condiûÏûçes para que ele ocorra, passando pelos diferentesô tipos de equilûÙbrio quûÙmico, como oô homogûˆneoô e oô heterogûˆneo, atûˋ as ferramentas matemûÀticas que o regem, como a constante de equilûÙbrio (K).
Abordaremos tambûˋm o famoso PrincûÙpio de Le Chatelier, que explica como fatores externos podem “deslocar” uma reaûÏûÈo.
Prepare-se para uma jornada completa, com exemplos prûÀticos e resoluûÏûçes de questûçes de vestibulares, para que vocûˆ chegue no dia da prova com toda a confianûÏa.
Em termos simples, oô equilûÙbrio quûÙmicoô ûˋ um fenûÇmeno que ocorreô exclusivamente em reaûÏûçes quûÙmicas reversûÙveis.
Imagine uma reaûÏûÈo onde os reagentes se transformam em produtos, mas os produtos tambûˋm podem se transformar novamente em reagentes. Eis, portanto, as reaûÏûçes quûÙmicas reversûÙveis.
Atente ao fato que, no inûÙcio, a velocidade da reaûÏûÈo direta (reagentes ã produtos) ûˋ alta. Conforme os produtos se acumulam, a velocidade da reaûÏûÈo inversa (produtos ã reagentes) comeûÏa a aumentar.
O equilûÙbrio, por conseguinte, ûˋ atingido no momento exato em queô essas duas velocidades se igualam.
û crucial, pois, entender que, no equilûÙbrio, as reaûÏûçes nûÈo param. Elas continuam ocorrendo nos dois sentidos, mas com a mesma velocidade. û o que se chama equilûÙbrio dinûÂmico.
Oô equilûÙbrio dinûÂmico acontece, portanto, quando uma reaûÏûÈo reversûÙvel tem suas velocidades direta (produtos) e inversa (reagentes) igualadas, mantendo as concentraûÏûçes constantes, embora as reaûÏûçes continuem ocorrendo simultaneamente.
Assim, do ponto de vista macroscû°pico, o que observamos ûˋ a constûÂncia das propriedades, como aô concentraûÏûÈoô de todas as substûÂncias envolvidas, que permanecem estûÀveis ao longo do tempo, embora nûÈo precisem ser iguais.
Importante salientar que, para que o equilûÙbrio seja estabelecido, algumas condiûÏûçes sûÈo necessûÀrias:
Aô quûÙmicaô estûÀ presente em cada detalhe da nossa vida, e o equilûÙbrio quûÙmico nûÈo ûˋ diferente.
Conhecer exemplos prûÀticos, por conseguinte, ajuda a solidificar oô conceitoô e a se sair bem no Enem, que adora questûçes contextualizadas. Vejamos, pois, alguns exemplos:
Abaixo imagem de garrafa sendo aberta que contûˋm ûÀgua com gûÀs. No momento em que se abre a garrafa, o equilûÙbrio quûÙmico ûˋ perturbado, liberando o gûÀs.

Uma das primeiras classificaûÏûçes que aprendemos sobre esse tema diz respeito ao estado fûÙsico dos participantes.
A depender disso, temos doisô tipos de equilûÙbrio quûÙmicoô principais. Vamos a eles:
Ocorre quando todos os participantes da reaûÏûÈo (reagentes e produtos) estûÈo na mesma fase, ou seja, apresentam uma û¤nica fase visûÙvel.
Isso ûˋ comum em reaûÏûçes onde todas as substûÂncias sûÈo gasosas ou estûÈo em soluûÏûÈo aquosa.
Exemplo clûÀssico: a reaûÏûÈo entre o gûÀs hidrogûˆnio e o gûÀs iodo para formar iodeto de hidrogûˆnio.
Hã(g) + Iã(g) ã 2 HI(g)
Neste caso, tudo estûÀ na fase gasosa.
Outro exemplo interessante ûˋ o equilûÙbrio entre o gûÀs castanho-avermelhado NOã (diû°xido de nitrogûˆnio) e o gûÀs incolor NãOã (tetrû°xido de dinitrogûˆnio):ô 2 NOã(g) ã NãOã(g).
Ao contrûÀrio do anterior, o equilûÙbrio heterogûˆneo envolve participantes em mais de uma fase.
Nesses sistemas, aô concentraûÏûÈoô de sû°lidos puros e lûÙquidos puros ûˋ considerada constante e, por isso,ô nûÈo entra na expressûÈo da constante de equilûÙbrio.
Exemplo: a decomposiûÏûÈo do carbonato de cûÀlcio (calcûÀrio) em û°xido de cûÀlcio (cal viva) e gûÀs carbûÇnico.
CaCOã(s) ã CaO(s) + COã(g)
Na expressûÈo da constante Kc para essa reaûÏûÈo, participa apenas o COã, pois os sû°lidos tûˆm “concentraûÏûÈo” constante e sûÈo incorporados ao valor de K. Por isso, escrevemosô Kc = [COã].
A interpretaûÏûÈo de grûÀficos ûˋ uma habilidade crucial para oô equilûÙbrio quûÙmico no Enem. Uma vez que sûÈo eles que nos ajudam a visualizar a dinûÂmica da reaûÏûÈo atûˋ que o equilûÙbrio seja atingido.
Basicamente, dois tipos de grûÀficos sûÈo mais comuns:
Nesse grûÀfico, observamos como as concentraûÏûçes de reagentes e produtos variam atûˋ a estabilizaûÏûÈo.
Abaixo, ilustraûÏûÈo de um grûÀfico mostrando a concentraûÏûÈo de reagentes diminuindo e a de produtos aumentando atûˋ ambas se tornarem constantes.
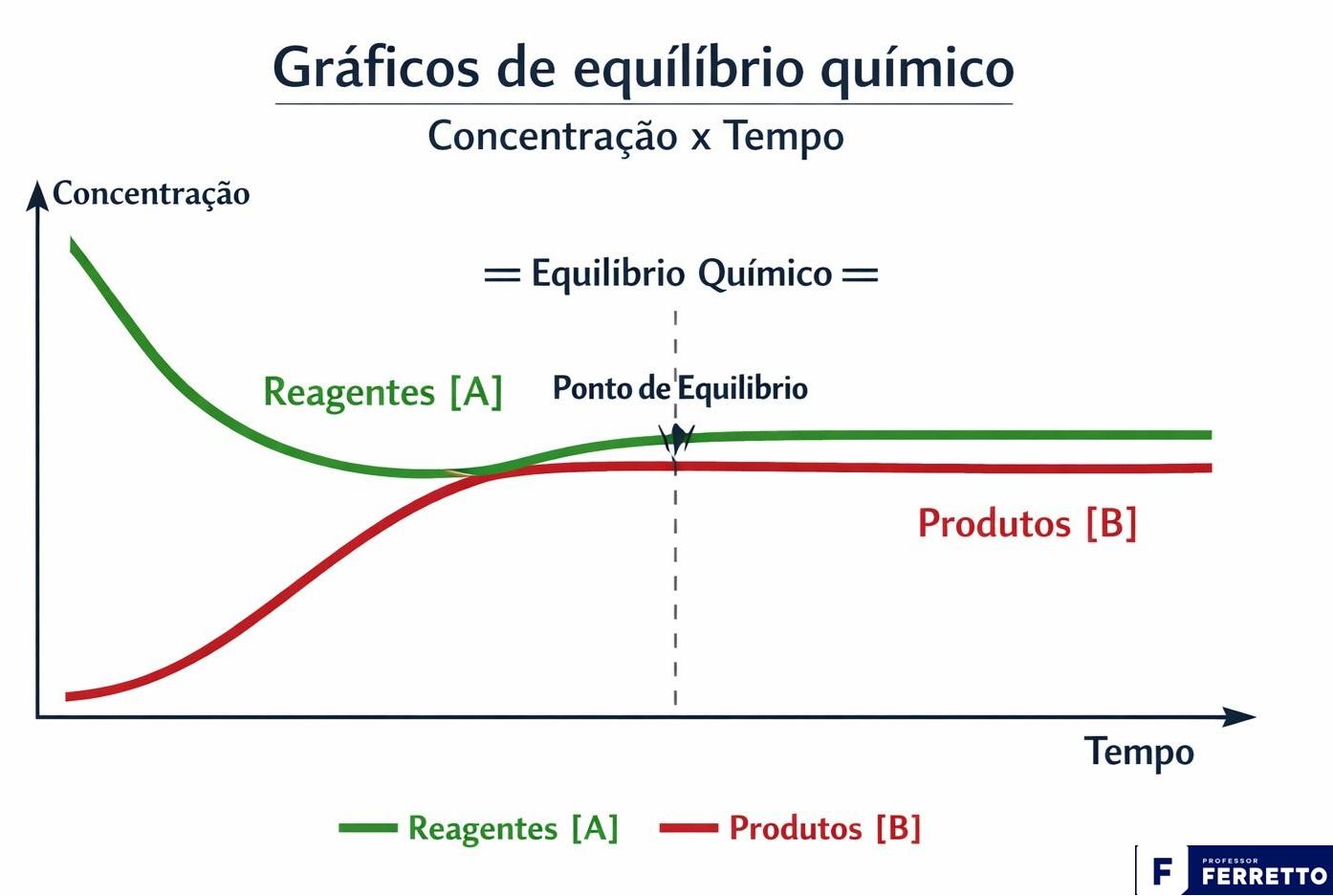
Esse grûÀfico, diferente do anterior, foca na cinûˋtica da reaûÏûÈo, isto ûˋ, a velocidade da reaûÏûÈo e os fatores que a influenciam.
Segue IlustraûÏûÈo de um grûÀfico com duas curvas: uma descendente (Vd) e uma ascendente (Vi) que se cruzam e se mantûˆm constantes.
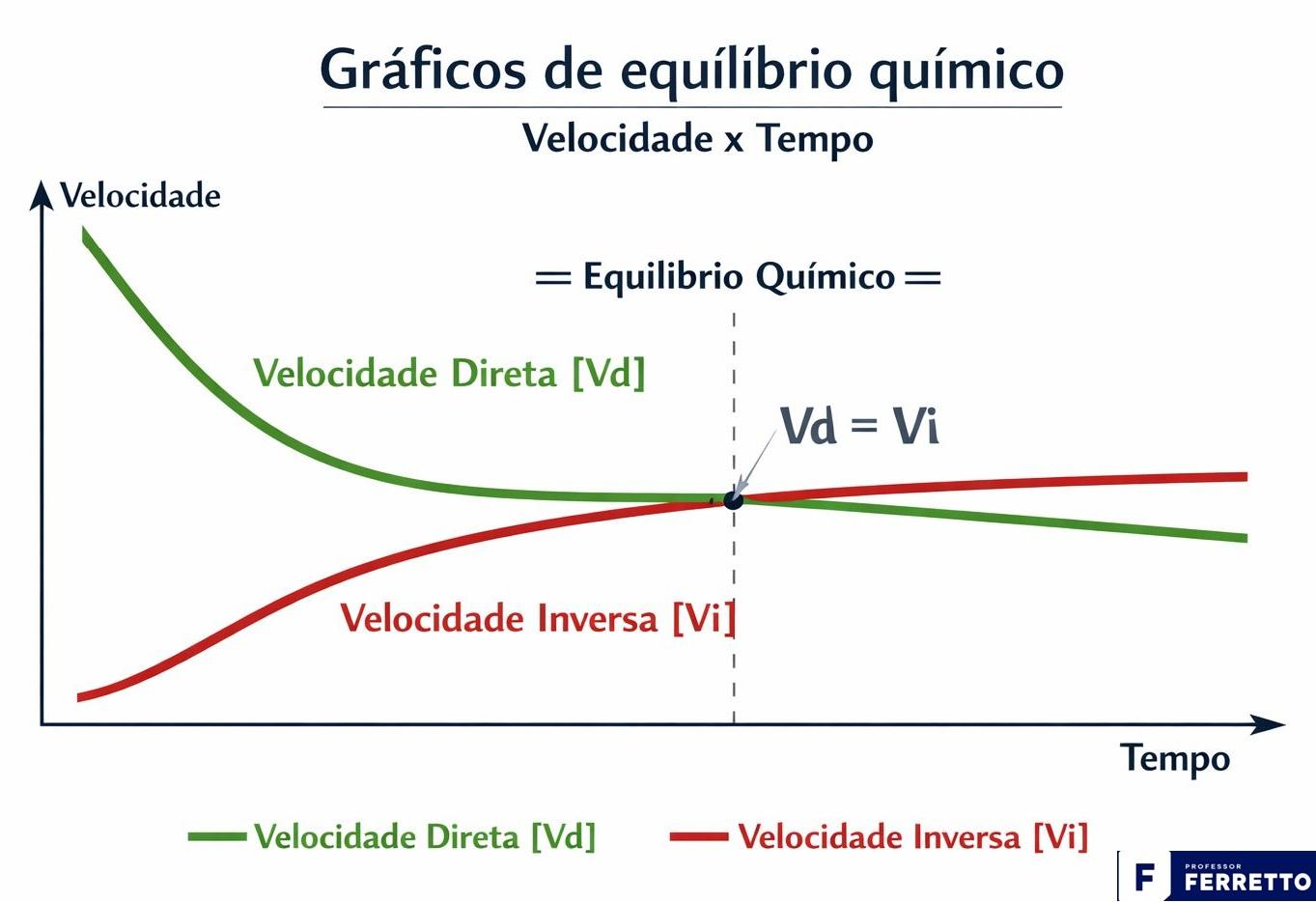
Para medir o equilûÙbrio, aô quûÙmicaô utiliza as constantes de equilûÙbrio e desenvolveu fû°rmulas para calculûÀ-la.
Por conseguinte, essas constantes nos dizem se a reaûÏûÈo ûˋ favorûÀvel û formaûÏûÈo de produtos ou se prefere manter os reagentes.
Importante salientar que o valor de K varia apenas com aô temperatura, diferente do equilûÙbrio que pode variar com a pressûÈo ou concentraûÏûÈo.
A seguir veremos essas constantes de equilûÙbrio e a relaûÏûÈo entre uma e outra.
Relaciona as concentraûÏûçes molares (mol/L) de produtos e reagentes no equilûÙbrio, cada uma elevada ao seu coeficiente estequiomûˋtrico.
Para uma reaûÏûÈo genûˋricaô aA + bB ã cC + dD, temos:
Kc = ([C]c x [D]d) / ([A]a x [B]b)
*Lembrando que [ ] representa a concentraûÏûÈo molar.
AtenûÏûÈo!ô Em equilûÙbrios heterogûˆneos, sû°lidos e lûÙquidos puros nûÈo entram na fû°rmula.
û utilizada nos cûÀlculos de equilûÙbrio quûÙmico quando hûÀ gases envolvidos.
A lû°gica ûˋ a mesma do Kc, mas usando as pressûçes parciais (p) dos gases no equilûÙbrio.
Kp = (pCc x pDd) / (pAa x pBb).
RelaûÏûÈo entre Kc e Kp: ûˋ possûÙvel relacionar as duas constantes pela fû°rmula:
Kp = Kc x (R x T)ön
Ondeô Rô ûˋ a constante dos gases,ô Tô ûˋ a temperatura em Kelvin, eô önô ûˋ a variaûÏûÈo do nû¤mero de mols gasosos (mols de produtos gasosos – mols de reagentes gasosos).
Indica o rendimento da reaûÏûÈo, ou seja, a porcentagem dos reagentes que efetivamente se converteram em produtos atûˋ o equilûÙbrio ser atingido.
O resultado pode ser multiplicado por 100 para se obter a porcentagem.
O grau de equilûÙbrio ûˋ muito û¤til para calcular rendimento de reaûÏûçes e graus de dissociaûÏûÈo. û, portanto, uma medida de consumo.
Para responder a essa pergunta, ûˋ importante levantar outro questionamento, qual seja, o que acontece quando se perturba um sistema que estûÀ em equilûÙbrio?
A resposta para esta pergunta ûˋ dada peloô PrincûÙpio de Le Chatelier: “Quando um fator externo age sobre um sistema em equilûÙbrio, este se desloca, procurando minimizar os efeitos dessa aûÏûÈo”.
Os principais fatores que causam esse deslocamento sûÈo:
Como visto acima, as principais fû°rmulas utilizadas no campo dos estudos do equilûÙbrio quûÙmico sûÈo as da constante de equilûÙbrio (Kc), do constante de equilûÙbrio em termos de pressûçes parciais (Kp) e grau de equilûÙbrio (öÝ).
Dominar as fû°rmulas ûˋ essencial! Vamos, pois, aplicûÀ-las em exemplos prûÀticos de questûçes do Enem e vestibulares para ver como elas funcionam.
Relembrando que a constante de equilûÙbrio relaciona as concentraûÏûçes molares (mol/L) de produtos e reagentes no equilûÙbrio.
Para realizar o cûÀlculo, vamos utilizar a questûÈo do Enem a seguir:
(Enem/2015)ô VûÀrios ûÀcidos sûÈo utilizados em indû¤strias que descartam seus efluentes nos corpos d’ûÀgua, como rios e lagos, podendo afetar o equilûÙbrio ambiental. Para neutralizar a acidez, o sal carbonato de cûÀlcio pode ser adicionado ao efluente, em quantidades apropriadas, pois produz bicarbonato, que neutraliza a ûÀgua. As equaûÏûçes envolvidas no processo sûÈo apresentadas:
(I)
(II)
(III)
(IV)
Com base nos valores das constantes de equilûÙbrio das reaûÏûçes II, III e IV a 25 ô¯C, qual ûˋ o valor numûˋrico da constante de equilûÙbrio da reaûÏûÈo I?
b) 5û10-5
c) 0,8û10-9
d) 0,2û105
e) 2,2û1026
ResoluûÏûÈo Passo a Passo:
Resultado Final:ô . Que ûˋ exatamente aô reaûÏûÈo I.
Resposta:ô O valor da constante de equilûÙbrio para a reaûÏûÈo I ûˋô ô (alternativa b)ô .
Relembrando tambûˋm que a fû°rmula da relaûÏûÈo entre Kp e Kc ûˋ utilizada nos cûÀlculos de equilûÙbrio quûÙmico quando hûÀ gases envolvidos.
Exemplo (adaptado UFRN):ô Sabendo-se que Kp = Kc (RT)ön, podemos afirmar que Kp = Kc para qual reaûÏûÈo?
a)ô COã(g) + Hã(g) ã CO(g) + HãO(g)
b) Hã(g) + ô§ Oã(g) ã HãO(l)
c) Nã(g) + 3 Hã(g) ã 2 NHã(g)
d) NO(g) + ô§ Oã(g) ã NOã(g)
Para Kp ser igual a Kc, ûˋ preciso que (RT)ön seja igual a 1, o que ocorre quando ön = 0. ön ûˋ a soma dos coeficientes dos produtos gasosos menos a soma dos coeficientes dos reagentes gasosos.
Logo:
COã(g) + Hã(g) ã CO(g) + HãO(g)ô -> ön = (1+1) – (1+1) = 0.ô Kp = Kc.
Resposta correta: alternativa a.
Por fim, temos a fû°rmula do grau de equilûÙbrio, que indica o rendimento da reaûÏûÈo, isto ûˋ, o percentual de reagentes que se converteram em produtos atûˋ o equilûÙbrio ser atingido.
Exemplo (adaptado FPS):
O pentacloreto de fû°sforo (PCl5), um composto quûÙmico sû°lido, sofre decomposiûÏûÈo (dissociaûÏûÈo) em fase gasosa e forma PCl3 mais Cl2.
Assim, se de 2 mols de PCl5 apenas 0,8 mols reagiram, qual o grau de equilûÙbrio? Em um recipiente fechado, 150 mols de um gûÀs X sofrem decomposiûÏûÈo,ô X(g) ã Y(g) + Z(g). No equilûÙbrio, restam 30 mols de A. Qual o grau de equilûÙbrio?
ResoluûÏûÈo:
Como o grau de equilûÙbrio (öÝ) ûˋ dado por:ô öÝ = (nô¯ de mols que reagiram) / (nô¯ de mols inicial), temos:
öÝ = 0,8 / 2 ÞÀˆ 0,4
Portanto, o grau de equilûÙbrio ûˋ 0,4 ou 40%.
PCl5 ã PCl3 + Cl2
Ressalte-se que o grau de equilûÙbrio (öÝ) ûˋ importante para definir concentraûÏûçes de equilûÙbrio ([C] = mol/l) e tambûˋm para calcular o Kc.
Agora que vocûˆ jûÀ revisou a teoria, deve estar se perguntando: como garantir que esse conhecimento se converta em pontos na prova?

A jornada rumo û aprovaûÏûÈo no Enem ou no vestibular exige, portanto, mais do que conhecer os conteû¤dos; ûˋ preciso saberô comoô estudûÀ-los de forma estratûˋgica e eficiente. û aûÙ que a metodologia certa faz toda a diferenûÏa.
Oô Professor Ferretto, pensando nisso, construiu uma plataforma de ensino que vai guiûÀ-lo por todo o percurso, incluindo o domûÙnio pleno sobre equilûÙbrio quûÙmico e os demais temas de quûÙmica e demais disciplinas.
A plataforma oferece videoaulas didûÀticas e objetivas, que explicam conceitos complexos de forma simples, acompanhadas de exercûÙcios comentados e umô plano de estudos personalizadoô que se adapta û s suas necessidades e ao seu tempo.
NûÈo deixe que dû¤vidas sobre conceitos, fû°rmulas ou cûÀlculos atrapalhem seu caminho para a universidade.
Invista na sua preparaûÏûÈo com quem tem um mûˋtodo comprovado!
Þô Acesse agora o curso gratuito do Professor Ferrettoô e experimente uma metodologia que jûÀ ajudou milhares de estudantes a alcanûÏarem sua aprovaûÏûÈo. Com videoaulas dinûÂmicas e uma linguagem clara, vocûˆ vai dominar aô quûÙmicaô de forma definitiva.
Þô Para um mergulho profundo e preparaûÏûÈo completa para o Enem, explore os planos do Enem Anatomy, que oferecem um cronograma de estudos personalizado e materiais exclusivos para vocûˆ garantir sua vaga na universidade dos sonhos.
Oô equilûÙbrio quûÙmicoô ûˋ, sem dû¤vida, um dos pilares daô quûÙmicaô e um dos temas mais recorrentes e desafiadores no Enem.
Vimos que ele vai muito alûˋm de uma simplesô definiûÏûÈoô de livro: estûÀ presente no ar que respiramos, nos alimentos que consumimos e em inû¤meros processos industriais.
Compreender a diferenûÏa entreô equilûÙbrio quûÙmico homogûˆneoô eô heterogûˆneo, saber interpretar grûÀficos, calcular as constantes (Kc e Kp) e, principalmente, dominar o PrincûÙpio de Le Chatelier para oô deslocamento do equilûÙbrioô sûÈo habilidades que farûÈo toda a diferenûÏa na sua prova.
NûÈo se trata apenas de memorizarô fû°rmulas, mas de enxergar a dinûÂmica do mundo ao seu redor.
Continue praticando, revisando os exemplos que resolvemos juntos e, sempre que possûÙvel, conectando a teoria com situaûÏûçes reais.
Dessa forma, vocûˆ estarûÀ nûÈo apenas preparado para as questûçes deô equilûÙbrio quûÙmico, mas tambûˋm para construir uma base sû°lida para seus estudos superiores.
Bons estudos e sucesso na sua jornada!

