
Os ciclos biogeoquĂmicos sĂŁo fundamentais para a sustentação da vida na Terra, envolvendo a circulação e transformação dos elementos quĂmicos...

Este artigo aborda de forma abrangente a definição de concentração de soluçÔes, tipos, suas aplicaçÔes no dia a dia, fĂłrmulas, exemplos prĂĄticos e exercĂcios com foco na preparação das provas do Enem e vestibulares.
O estudo da concentração de soluçÔes Ă© um tema essencial para alunos que buscam entender melhor fenĂŽmenos quĂmicos e aplicar esse conhecimento em situaçÔes prĂĄticas, como a correta dosagem de medicamentos e a preparação de soluçÔes. Este artigo aborda de forma abrangente a definição de concentração de soluçÔes, suas aplicaçÔes no dia a dia e nos exames do ENEM e vestibulares, alĂ©m de detalhar os principais tipos de concentração: comum, molar, tĂtulo e partes por milhĂŁo. A importĂąncia de dominar essas fĂłrmulas e conceitos Ă© reforçada pelos exemplos prĂĄticos e exercĂcios tĂpicos presentes nos exames. O guia explora em profundidade cada tipo de concentração, oferecendo fĂłrmulas detalhadas e exemplos de aplicação prĂĄtica. Entre os pontos abordados estĂŁo a diferença entre concentração molal e molaridade, a importĂąncia de entender a densidade, e a relação entre diferentes tipos de concentração. A seção final destaca estratĂ©gias de estudo para dominar este assunto, incluindo a prĂĄtica ativa atravĂ©s de exercĂcios e o uso de materiais de estudo estruturados. Com foco na preparação para o ENEM, o artigo contĂ©m dicas Ășteis para o cĂĄlculo de concentraçÔes e discute como o tema pode ser cobrado nos exames. A conclusĂŁo reforça a necessidade de prĂĄtica constante para a compreensĂŁo dos conceitos e sucesso nos vestibulares.
O estudo da concentração de soluçÔes responde a perguntas como, por que o soro caseiro tem uma quantidade especĂfica de sal e açĂșcar, ou como um medicamento injetĂĄvel Ă© preparado com a dose exata?
Dominar esse tema Ă© fundamental nĂŁo apenas para o seu dia a dia, mas tambĂ©m para garantir uma Ăłtima pontuação nas provas de QuĂmica do ENEM e dos principais vestibulares do paĂs.
Entender a concentração de soluçÔes é aprender a resolver problemas prĂĄticos, interpretar rĂłtulos, compreender fenĂŽmenos quĂmicos e, por consequĂȘncia, garantir pontos preciosos na sua prova.
Neste guia vocĂȘ aprenderĂĄ “o que Ă© concentração de soluçÔes“, “como calcular concentração de soluçÔes” e “quais as principais fĂłrmulas e tipos“.
Prepare-se para uma imersĂŁo completa no universo da concentração de soluçÔes quĂmicas e saia na frente na sua preparação. Vamos lĂĄ, mergulhe conosco!
Em QuĂmica, uma solução Ă© uma mistura homogĂȘnea formada por duas ou mais substĂąncias.
A substùncia que estå dissolvida na solução é o soluto, enquanto o solvente é a substùncia que dissolve.
A imagem abaixo ilustra uma solução quĂmica a partir da mistura do soluto com o solvente.

A concentração de soluçÔes, por sua vez, é a medida da quantidade de soluto presente em uma determinada quantidade de solvente ou de solução.
Em outras palavras, Ă© a forma de expressar se uma solução Ă© “forte” (concentrada) ou “fraca” (diluĂda).
Existem diversas maneiras de expressar essa relação, cada uma com sua aplicação especĂfica, como veremos a seguir.
Como visto acima, a concentração Ă© a razĂŁo entre soluto e solvente em uma solução quĂmica. HĂĄ, no entanto, diversas maneiras de se medir essa concentração.
Vamos, portanto, explorar os principais tipos de concentração de soluçÔes quĂmicas que vocĂȘ precisa dominar para a prova.
A concentração comum (C), também chamada de concentração em g/l, é a relação entre a massa do soluto (em gramas) e o volume da solução (em litros).
à uma das formas mais simples e diretas de se expressar a fórmula de concentração de soluçÔes.
FĂłrmula:
C = m / V
Onde:
Exemplo prĂĄtico: se vocĂȘ dissolve 20 g de cloreto de sĂłdio (NaCl) em ĂĄgua suficiente para preparar 500 ml (0,5 l) de solução, qual a concentração comum?
Aplicando a fĂłrmula:Â
C = 20 g / 0,5 l = 40 g/l.
Isso significa que em cada litro dessa solução, hå 40 gramas de sal.
A molaridade (M) Ă© uma das formas mais cobradas em vestibulares. Ela relaciona o nĂșmero de mols do soluto com o volume da solução em litros.
O mol é a unidade que usamos para quantificar a matéria e sua massa (massa molar, em g/mol) é encontrada na tabela periódica.
Para deixar mais claro, o mol sĂŁo exatamente 6,022 x 10ÂČÂł entidades elementares, como molĂ©culas ou ĂĄtomos de uma substĂąncia ou elemento.
A concentração molar ou molaridade, portanto, é uma ferramenta essencial para a estequiometria.
FĂłrmula:
M = nâ / V ou M = m / (Mâ · V)
Onde:
Exemplo pråtico: uma solução de hidróxido de sódio (NaOH) tem 4 g dessa base dissolvidos em 500 ml de solução. Sabendo que a massa molar do NaOH é 40 g/mol, qual a molaridade?
1Âș) Transformar o volume para litros: 500 ml = 0,5 l.
2Âș) Aplicar a fĂłrmula:
M = 4 g / (40 g/mol · 0,5 l) = 4 / 20 = 0,2 mol/l.
O tĂtulo (Ï) Ă© uma forma de expressar a concentração adimensional (sem unidade) que relaciona a massa do soluto com a massa total da solução (soluto + solvente).
Como anotado, a massa em tĂtulo Ă© adimensional e varia de 0 a 1, ao passo que a porcentagem em massa varia de 0 a 100.
Essa notação é mais comum em dosagem de medicamentos, concentração de algumas substùncias como o soro fisiológico e nas soluçÔes para experimentos ou anålises.
FĂłrmula:
Ï = mâ / m ouÂ Ï = mâ / (mâ + mâ)
Onde:
Para obter a porcentagem em massa, multiplica-se o tĂtulo por 100 (% = Ï Â· 100).
Talvez vocĂȘ jĂĄ tenha visto a seguinte notação %(m/m). O que Ă© isso?
Essa notação significa “porcentagem massa por massa” e Ă© exatamente o tĂtulo em porcentagem.
Por exemplo, um rĂłtulo que diz “soro fisiolĂłgico 0,9% (m/m)” indica que existem 0,9 g de NaCl para cada 100 g de solução.
Quando a solução Ă© extremamente diluĂda, usar porcentagem se torna inviĂĄvel.
Para esses casos, utilizamos a notação partes por milhão (ppm), que indica quantas partes de soluto existem em 1 milhão de partes de solução.
Ă muito usada para expressar concentraçÔes de poluentes na ĂĄgua ou no ar, e de nutrientes em soluçÔes agrĂcolas.
FĂłrmula conceitual:
1 ppm = 1 g de soluto / 1.000.000 g de solução
Para soluçÔes aquosas diluĂdas, como 1 l de ĂĄgua tem aproximadamente 1000 g, 1 ppm equivale a cerca de 1 mg/l.
Exemplo prĂĄtico: a Rifampicina Ă© um antibiĂłtico utilizado no tratamento da tuberculose, hansenĂase, meningite, entre outros. Esse poderoso antibiĂłtico costuma conter o contaminante MNP (1-metil-4-nitrosopiperazina) e a ingestĂŁo aceitĂĄvel desse contaminante Ă© regulada em partes por milhĂŁo e gira em torno de 1,5 ppm. Isso significa que em 1kg desse antibiĂłtico sĂł pode ter 1,5 mg de MNP.
Abaixo imagem sobre o conceito de concentração de solução expressa em partes por milhão (ppm), comumente utilizada para medição de poluentes no ar e na ågua.

A concentração molal, ou a molalidade (W), Ă© a relação entre o nĂșmero de mols do soluto e a massa do solvente em quilogramas.
Cuidado para nĂŁo confundir molalidade (W) com molaridade (M) que jĂĄ foi vista acima.
Diferente da molaridade, portanto, a molalidade nĂŁo depende da temperatura, pois o volume pode variar com o aquecimento, mas a massa do solvente permanece constante.
Ă uma unidade fundamental no estudo das propriedades coligativas.
FĂłrmula:
W = nâ / mâ ou W = (1000 · mâ) / (mâ · Mâ)
Onde:
Exemplo prĂĄtico:Â se 0,6 mol de um soluto Ă© dissolvido em 480 g (0,48 kg) de ĂĄgua, a molalidade serĂĄ:Â
W = 0,6 mol / 0,48 kg = 1,25 mol/kg.
A densidade de uma solução é a relação entre a massa da solução (soluto + solvente) e o seu volume, geralmente expressa em gramas por mililitro (g/ml).
De se ver, portanto, que, embora não seja uma medida de concentração pura, a densidade (d) é uma propriedade importante que se relaciona com ela.
FĂłrmula:
d = m / V
Onde:
Exemplo pråtico: a densidade da solução de hidróxido de sódio (NaOH) de 1 M é de aproximadamente 1,24 g/ml para uma concentração de 40% em massa de soluto. A densidade aumenta com a concentração, o que isso significa? Significa que cada mililitro dessa solução de NaOH tem massa de 1,24g.
Atenção para não confundir!
Na concentração comum (C), usamos a massa do soluto. Na densidade, usamos a massa de toda a solução.
Sim, pois as medidas que expressam a concentração das soluçÔes podem se correlacionar, tornando-se um elemento Ăștil e poderoso no estudo da concentração de soluçÔes.
Por essa razĂŁo, uma fĂłrmula muito Ăștil, especialmente em exercĂcios de Enem e vestibulares, Ă© a que conecta a concentração comum (C), a densidade (d) da solução e o tĂtulo (Ï).
Fórmula de relação:
C = 1000 · d · Ï
Onde:
Essa fórmula só é vålida se a densidade estiver em g/ml. O fator 1000 é usado para ajustar as unidades, pois 1 l = 1000 ml.
Por conseguinte, essa relação permite, por exemplo, encontrar a molaridade a partir do tĂtulo e da densidade, mostrando como os conceitos sĂŁo interligados.
Enquanto vocĂȘ estuda o tema concentração de soluçÔes, podem surgir algumas dĂșvidas sobre pontos que talvez nĂŁo lhe tenham ficado muito claros.
Abaixo apresentamos as respostas para alguns desses possĂveis questionamentos.
Embora existam vĂĄrios, os trĂȘs mais comuns e frequentemente citados sĂŁo: Concentração Comum, Molaridade e TĂtulo.
Como visto acima, ainda temos a concentração expressa em partes por milhão (ppm) e a concentração por mol, ou molalidade.
Talvez essa pergunta contenha certo equĂvoco, pois, conforme visto acima, hĂĄ os cinco tipos de concentração, isto Ă©, 5 maneiras diferentes de se medir a concentração de uma solução quĂmica.
Por consequĂȘncia, a pergunta que deve ser feita Ă©, quais sĂŁo os cinco tipos de concentração de soluçÔes quĂmicas?
JĂĄ as soluçÔes quĂmicas podem ser classificadas de acordo com o estado fĂsico (sĂłlidas, lĂquidas, gasosas), o nĂvel de solubilidade (insaturadas, saturadas, supersaturadas etc.).
Para que vocĂȘ nĂŁo fique em dĂșvida e nĂŁo corra o risco de confundir esses conceitos, confira nosso artigo especĂfico sobre soluçÔes quĂmicas.
A concentração Ă© medida atravĂ©s das fĂłrmulas especĂficas de cada tipo, utilizando unidades como g/l, mol/l, porcentagem (%), ppm etc., conforme ilustrado acima quando se trata dos tipos de concentração de soluçÔes.
O cålculo de concentração de soluçÔes é uma habilidade que se desenvolve com a pråtica e a atenção a alguns detalhes cruciais.
Segundo uma anĂĄlise de mais de 20 anos de provas da Fuvest, Unicamp e ENEM, os conceitos de soluçÔes e estequiometria aparecem consistentemente entre os tĂłpicos mais recorrentes, figurando em cerca de 15% a 20% das questĂ”es de QuĂmica.
Dominar esse assunto, portanto, é um passo estratégico para garantir uma boa colocação.
No infogråfico abaixo estão algumas dicas para calcular corretamente a concentração de soluçÔes.
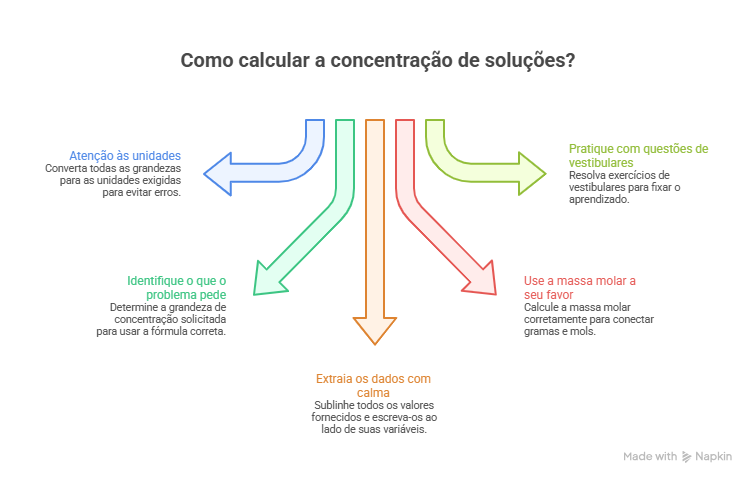
O Enem e os vestibulares tradicionais adoram contextualizar a QuĂmica.
Em consequĂȘncia, dificilmente vocĂȘ verĂĄ uma questĂŁo perguntando “Qual a fĂłrmula da molaridade?”.
Em vez disso, o tema aparece inserido em situaçÔes do cotidiano, experimentos ou processos industriais.
Vamos analisar alguns exemplos de concentração de soluçÔes exercĂcios tĂpicos:
(Enem â adaptada) â O Soro fisiolĂłgico contĂ©m 0,900 gramas de NaCl, massa molar=58,5g/mol, em 100 ml de solução aquosa. A concentração do soro fisiolĂłgico, expressa em mol/l, Ă© igual a:
a) 0,009
b) 0,015
c) 0,100
d) 0,154
e) 0,900
Resolução comentada:
(ITA-SP â adaptada) – O rĂłtulo de um frasco diz que ele contĂ©m solução 1,50 molal de LiNO3 em etanol. Isto quer dizer que a solução contĂ©m:
a) 1,50 mol de LiNO3/quilograma de solução.
b) 1,50 mol de LiNO3/litro de solução.
c) 1,50 mol de LiNO3/quilograma de etanol.
d) 1,50 mol de LiNO3/litro de etanol.
e) 1,50 mol de LiNO3/mol de etanol.
Resolução comentada:
Esta questão testa o conhecimento da definição exata de molalidade.
A molalidade (W) Ă© definida como o nĂșmero de mols de soluto por quilograma de solvente. No caso, o soluto Ă© o LiNO3 e o solvente Ă© o etanol.
Portanto, uma solução 1,50 molal contém 1,50 mol de LiNO3 para cada quilograma de etanol.
Resposta: alternativa c).
Dominar a concentração de soluçÔes fórmulas e conceitos é uma jornada que exige método e as ferramentas certas.
A simples leitura nĂŁo Ă© suficiente; Ă© preciso praticar ativamente e revisar constantemente.
Para isso, recomendamos alguns passos cruciais como mapas mentais, resolução de exercĂcios e um bom cronograma de estudos, conforme ilustrado na imagem abaixo.
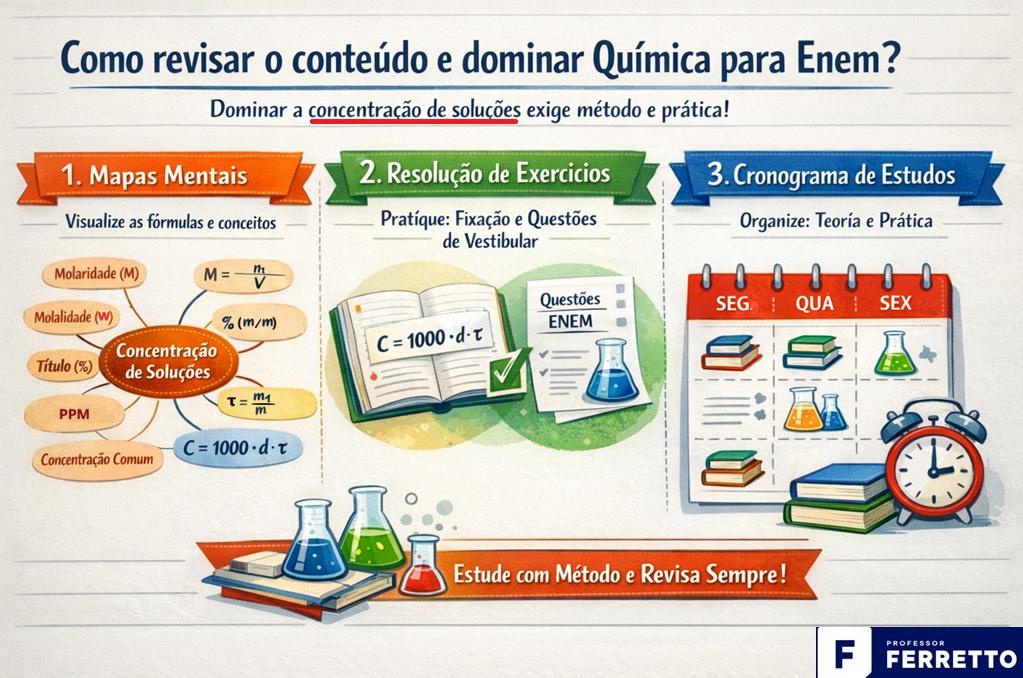
đ Quer ir alĂ©m? NĂŁo perca mais tempo reunindo material fragmentado. Comece hoje mesmo a estudar com quem entende do assunto.
No Professor Ferretto, vocĂȘ encontra um curso completo focado 100% no Enem e vestibulares. Aprenda com a metodologia que jĂĄ aprovou milhares de estudantes em todo o Brasil.
đ Acesse nosso curso gratuito e experimente a metodologia
đ Quer se preparar com as orientaçÔes completas do conteĂșdo para o Enem? Garanta seu acesso!
A concentração de soluçÔes é um pilar fundamental da QuĂmica e um tema comumente presente nas provas do Enem e vestibulares.
Ao longo deste guia, exploramos os principais tipos de concentração de soluçÔes quĂmicas. Vimos suas fĂłrmulas de concentração de soluçÔes, aplicaçÔes, bem como, a relação entre eles.
Verificamos que, mais do que memorizar, Ă© preciso entender o conceito por trĂĄs de cada expressĂŁo e estar atento Ă s unidades de medida.
Por isso, a prĂĄtica com exercĂcios, como os exemplos resolvidos, Ă© um caminho eficaz para a compreensĂŁo do tema e ganhar segurança.
Cada questão sobre diluição e concentração de soluçÔes ou sobre como calcular concentração de soluçÔes resolvida é uma oportunidade para chegar mais próximo à aprovação.
Por fim, estudar através de curso com método reconhecido na aprovação do Enem e vestibulares, pode ser sua melhor aposta.
Bons estudos e sucesso na sua jornada!

